대구카톨릭대 김종기 교수 연구팀이 투과성 양성자를 이용해 알츠하이머성 뇌의 신경독성 제거 및 분쇄 기술을 개발했다.
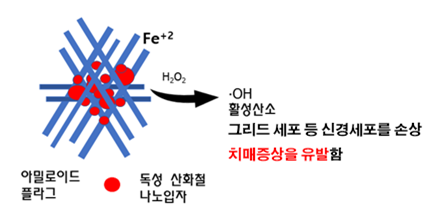
아밀로이드 플라그 내 독성 산화철의 활성산소 생성
알츠하이머 치매의 신경독성은 베타 아밀로이드와 타우 단백질 응집에 의해 발생한다고 알려져 있다.
아밀로이드와 타우 단백질이 산화철 나노입자와 복합체를 형성하고, 이 때 반응성이 큰 2가 철이온(Fe+2)으로 인해 활성산소가 생성되면서 독성이 유발된다.
연구팀은 투과성이 있는 양성자를 조사하여, 정상 뇌세포의 손상없이 신경독성을 제거하는 쿨롱 나노킬레이트 치료법을 개발했다.
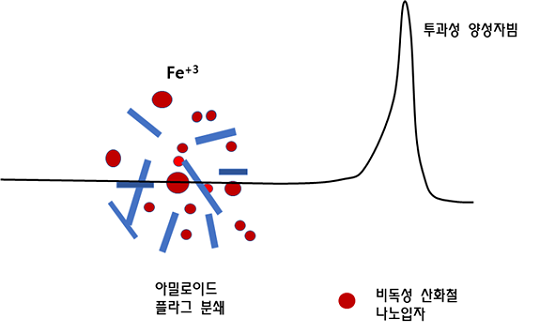
투과성 양성자를 조사하여, 산화철나노입자로부터 아밀로이드 플라그가 분쇄되면서, 산화철이 비독성 3가 이온으로 변환되는 모습.
쿨롱 나노킬레이트란 양성자-전자 간 쿨롱 상호작용으로 산화철 나노입자로부터 전자 방출이 유도됨으로써 단백질과 결합구조가 와해되고 철의 독성이온이(Iron(II)) 원래 특성대로 비독성화되는(Iron(III)) 과정을 말한다.
양성자에 의해 베타 아밀로이드와 산화철의 결합이 와해되고, 2가 철이온(Fe+2)은 독성이 없는 3가 철이온(Fe+3)으로 변환된다.
기존 연구들이 아밀로이드 플라그나 타우 매듭 중 하나만 표적으로 하는 반면, 이 치료기술은 베타 아밀로이드-산화철 결합체가 타우 응집체의 주 성분이므로 양성자에 의해 두 종류의 표적을 동시에 제거할 수 있다.

김종기 교수
김종기 교수는 “이 연구는 투과성 양성자를 이용 알츠하이머성 뇌의 신경독성 및 플라그‧매듭을 제거하는 기반 기술을 개발한 것이다”라고 연구의 의의를 설명하며, ”향후 생체모델을 이용해 노인반 및 타우 매듭의 그리드 세포 손상 경로와 노인반‧타우 매듭 제거에 따른 인지기능 회복 및 치료 안전성을 연구할 계획“이라고 밝혔다.
알츠하이머성 치매의 신경독성유발 아밀로이드 플라그, 타우 매듭을 비침습적으로 동시에 제거하는 치료 기술로 활용될 수 있다.
또 산화철나노입자를 매개로 단백질침착이 유발되는 여러 퇴행성 뇌질환 (파킨슨 질환 등) 치료에 적용 가능하다.
이 연구는 국제학술지 케임브리지 재료연구회 교신(MRS communications) 6월 15일 논문으로 게재되었다. (논문명:nvestigation of the redox state of magnetite upon Aβ-fibril formation or proton irradiation; implication of iron redox inactivation and β-amyloidolysis)
ilyo08@ilyo.co.kr