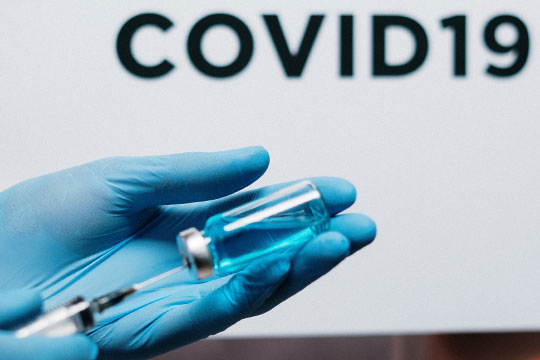
식품의약품안전처는 25일 화이자의 코로나19 백신의 품목허가 신청이 접수됐다고 밝혔다.
이번에 허가 신청한 백신은 미국 화이자가 독일 바이오엔텍과 공동으로 개발한 mRNA(메신저 리보핵산) 백신이다. 코로나19 바이러스의 항원 유전자를 mRNA 형태로 주입해 체내에서 항원 단백질을 생성함으로써 면역반응을 유도하는 백신이다.
mRNA 백신은 제조 기간이 짧아 단기간 내 대량생산이 가능하나 RNA 분해효소에 의해 주성분인 mRNA가 쉽게 분해되는 등 안정성이 좋지 않아 초저온 냉동의 콜드체인이 필요하다.
화이자 백신의 예상 접종 대상자는 만 16세 이상이다. 예상용법은 1회 접종 후 3주 후에 추가 접종하며 보관조건은 영하 60~90℃에서 6개월로 신청됐다.
화이자 백신은 전 세계 28개 규제기관에서 긴급사용승인 또는 조건부 허가를 받았다. 세계보건기구(WHO) 외에 영국, 미국, 캐나다 등 21개 국가가 긴급사용을 승인했으며 유럽연합(EU)과 스위스 등 5개 국가는 허가 후 자료를 추가로 제출하도록 조건부 허가했다.
박형민 기자 godyo@ilyo.co.kr